全球首例!把猪心移植给患者,终于做到了
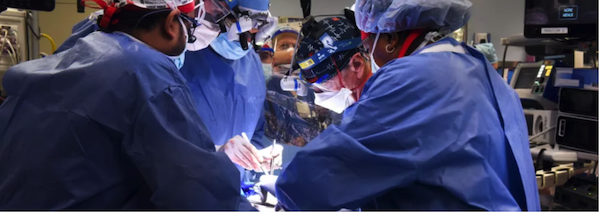
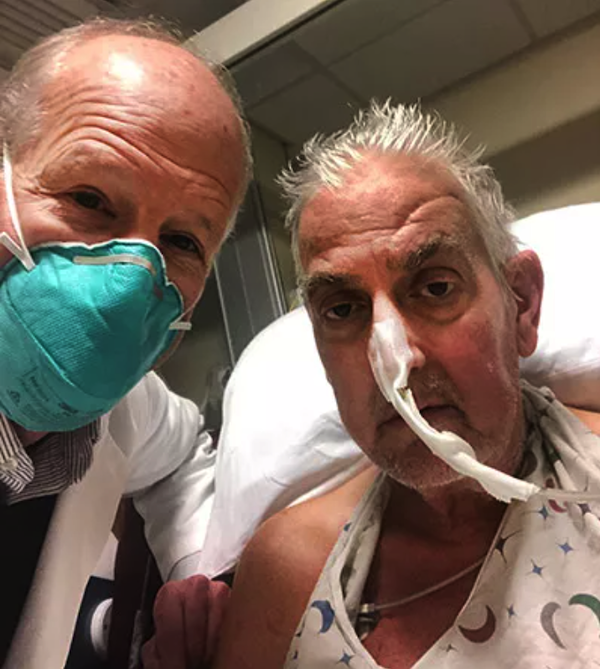
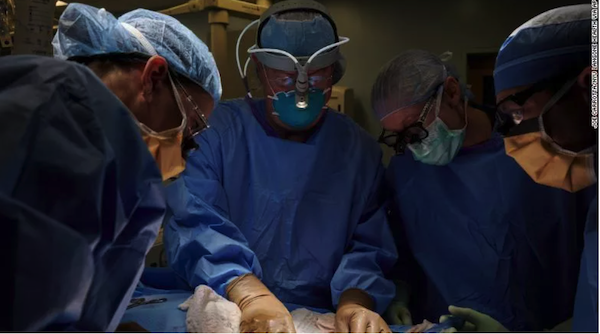
57岁的大卫·贝内特(David Bennett)完成了一次“实验性”心脏移植手术。为其捐献心脏的,是一头1岁大、重240磅的“基因修饰”猪。基因修饰是使用分子生物学技术,去除动物基因中易引起排异反应的部分,使移植的动物器官能与人体相容并长期存活。执行该手术的美国马里兰大学医学中心(以下简称UMMC)官宣,这是全球首例人移植转基因猪心手术。当地时间1月10日,术后第3天。UMMC心脏移植项目主任巴特利·格里菲斯医生(Bartley Griffith)表示,贝内特仍需体外膜肺氧合(ECMO),替代一部分心脏泵血功能,但总体情况稳定、良好,没有发生超急性免疫反应。图片来源于University of Maryland Medical Center“要么死,要么移植猪心。”UMMC新闻稿显示,术前1天,贝内特称非常清楚自己的状态。他表示,自己曾接受过猪瓣膜移植,最爱吃的食物就是培根。“这是一次豪赌,也是我活下去的最后选择。”“但如果可以,还是希望移植一颗人类的心脏。”贝内特因患复杂性遗传性心脏病,致终末期心衰。2020年10月,其身体状况突然恶化,因危及生命的心律失常入院。他的治疗方案制定艰难。包括UMMC在内,多家美国移植中心评估认为,贝内特的心律失常严重,不适合植入人工心脏。但其基础情况又没资格进入器官移植等候名单。大卫·贝内特(David Bennett,右)和医疗团队合影。/University of Maryland Medical Center即使进了名单,贝内特能及时等到器官的机会,也很低。根据美国器官共享联合网络(UNOS)统计,2021年,约有41354名美国人接受器官移植,其中有3,800多例属心脏移植。20:1——这是全球急需器官移植的患者数量,与所捐献器官数量的比值。“20”还不包括那些靠药物维持能拖日子、但终究要移植的患者们。根据美国政府数据,每天约有17人在等待器官中离世。UMMC提出“另一种可能”:异种器官移植,使用动物器官完成救命手术。猪心脏在保存和移植过程中,必须使用特殊溶液灌注,才能保证活性。/University of Maryland Medical CenterBBC报道,异种器官移植最早或可追溯到1682年。当时,荷兰外科医生乔布·简斯祖·范·米克伦(Job Janszoon van Meekeren)称,自己修复一名士兵的头骨时,用了一片狗骨头碎片。教会闻讯后要求其立刻取出,但发现伤口已经愈合。这名士兵的后续情况暂未可知。但全球医学科学家对异种移植的探索,从未停止。1905年,法国完成世界首例兔肾薄片人体移植手术。受体是一名肾功能衰竭患儿。术后16天,患儿死于排异反应引发的肺部感染。次年,还是在法国,一只猪的肾脏和一只山羊的肝脏,被分别移植到两名女性患者体内。两人在术后不久死亡,死因是服用免疫抑制药物致严重感染。1984年、1992年,医生们分别用狒狒的心脏、肝脏进行人体移植。术后数周内,病患死于排异反应。2003年,异种移植进入新阶段。美国Revivicor公司创造性地在克隆猪身上,进行基因修饰,培育出第一代“医用猪”。这被美国《发现》杂志列为当年百项重大科学发现之一。Revivicor这个名字可能不为人熟知,但其前身PPL Therapeutics生物技术公司声名显赫——全球第一只克隆羊“多莉”的创造者。Revivicor公司于2020年12月提供的一只基因修饰猪照片。该司未声明照片拍摄时间。/AP问题来了:为啥Revivicor公司选择偶蹄目猪做研究,但放弃在物种、生理解剖等方面,和人类相似的猩猩、狒狒等灵长目动物?Revivicor公司分析指出,因为“二师兄”好用。猪和人在食性、代谢水平等方面接近,体温、心率近似。一些猪器官的“性能参数”也和人类相近。比如,猪心与人类心脏的大小差不多,管道分布和动力输出也类似。此外,灵长目动物的世代间隙长。尤其是猩猩和狒狒,10年一代,一胎一仔,饲养成本高。而猪是一养一窝,一年多就长熟了,适合定向育种和大规模繁殖。更重要的是,猩猩、狒狒是人类“近亲”。其体内存在的一些病毒,如猴免疫缺陷病毒等,易传染给人类。将它们的器官移植到人体后,可能会孵化出更厉害的病毒。而猪体内的病毒不易感染人类。2015年,美国哈佛大学研究团队通过基因编辑技术,敲除猪种群基因组里的PERV(内源性逆转录病毒),更是扫清猪器官移植的感染隐患。此前研究表明,含PERV类病毒的猪细胞在与人类组织共同孵育时,存在被激活并感染人类细胞的风险。猪是异种器官移植的最佳选择对象,成为国际共识。目前,猪心脏瓣膜、猪胰腺细胞都已成功进入人体。猪皮也被用作烧伤患者的临时移植物。2018年12月,《自然》发表一项重磅成果称,德国慕尼黑沃尔特·布兰达尔(Walter Brendel)实验医学中心的布鲁诺·莱哈特(Bruno Reichart)团队,成功将基因修饰后的猪心脏移植到狒狒体内。最长存活时间为6个月。两年后,《循环》杂志发表美国麻省总医院文章称,猪心有望成为人类心脏移植供体。该文预测,人类或最早于2021年底,接受猪心移植。2021年12月31日,美国食品药品监督管理局(FDA)通过“同情使用”条款,授予大卫·贝内特实验性手术的“紧急授权”。术中使用到的猪心供体,就来自Revivicor公司。UMMC称,这头具有奉献精神的猪,接受了10处独特的基因修改。包括敲除3个基因,以降低人体免疫系统的攻击性排异反应。敲除1个生长基因,以防止移植后猪心继续生长。此外,6个人类基因被编辑、插入供体猪的基因组内。目的是让猪的器官对人类免疫系统更耐受。UMMC还用到一款创新药物,预防器官移植手术后的排异反应。UMMC表示,经过基因修饰的动物器官在贝内特的体内发挥作用,没有立即被排异。这场手术的成果很可能改变全球许多人的命运。“我们从没在人类身上做过这种事。我认为,我们给了他(贝内特)一个比继续用药更好的治疗选择。”主刀医生巴特利·格里菲斯医生说,但远期风险和收益全部未知。“他能活一天、一周、一个月还是一年,我不知道。”“这是一个分水岭性质的事件。”美国纽约大学朗格尼医学中心移植研究所主任罗伯特·蒙哥马利(Robert A Montgomery)表示。2021年10月,在征得患者家属同意的情况下,罗伯特·蒙哥马利也完成了一台异种器官移植手术。他给一名脑死亡的终末期肾病患者,移植一头转基因猪的肾脏。该手术过程与实际移植有所区别。猪肾并未被植入患者体内,而是在腹部外侧、和大腿血管相连。手术团队解释,这是因为在异种移植中,问题常发生在人体血管和动物器官吻合处。“移植器官几乎立刻开始正常运作。”蒙哥马利告诉《纽约时报》,器官在体外发挥作用的事实,有力地表明它在体内也会很能干。2021年10月,全球首例转基因猪肾人体移植手术完成。/AP针对病友和媒体们普遍关心的“异种移植何时广泛推广”,UMMC团队表示,还有许多问题需要回答。根据国际异种移植指导委员会意见,异种移植研究进入临床的前提是,60%的动物实验受体存活时间超过3个月,至少有10例连续的移植实验。而临床试验的目标是:永久性替换原有器官,必须有超过50%的受体生存时间长于6个月。“如果成功,基因修饰猪可能成为一种可持续、可再生的器官来源,相当于器官供应的太阳能和风能。”蒙哥马利告诉《纽约时报》。目前,这些“医用猪”的产能、生产许可等,已有保障。2020年12月,美国FDA给Revivicor公司的基因修饰猪GalSafe,发了上市许可。与常规猪不同,GalSafe猪被敲除了细胞表面的α-半乳糖分子。这一分子广泛存在于猪、羊、牛等“红肉”动物的细胞表面。有些人吃红肉会出现过敏反应,就都赖它。除了让人过敏,α-半乳糖分子也是导致免疫排异反应的主要原因之一。因为进化到灵长目动物后,体内就不带半乳糖了。据FDA介绍,GalSafe猪既能直接食用,也能用于加工、生产不含α-半乳糖的医疗产品,如血液稀释药物肝素。Revivicor最希望通过GalSafe猪实现的,就是生产用于异种移植的器官。时间再往前推。2017年,全球最大的猪肉生产商史密斯菲尔德食品公司宣布,新组建一个独立的生物科学单元,专门饲养“医用猪”,希望形成用于人体移植的猪器官生产链。据称,这些猪都是剖腹产的,一出生就马上和猪妈妈分开,被送入超洁净猪舍,接受人工饲养。猪舍内无菌、无毒,饲养人员进去前要沐浴更衣。总而言之,它比某些人还干净。1.In a medical first, a man with terminal heart disease gets a transplant of genetically modified pig heart. CNN2.University of Maryland School of Medicine Faculty Scientists and Clinicians Perform Historic First Successful Transplant of Porcine Heart into Adult Human with End-Stage Heart Disease. Universty of Maryland School Of Medicine3.US Surgeons Transplant Pig Heart Into Human Patient. Huffpost4.A pig medical milestone. USA Today5.US surgeons successfully test pig kidney transplant in human patient. CNN6.Progress Toward Cardiac Xenotransplantation. Circulation. 2020;142:1389–1398. doi.org/10.1161/CIRCULATIONAHA.120.048186