抗生素耐药现状
多年来,抗生素耐药(AMR)被视为全球人类健康的重大威胁之一。
当地时间1月20日,《柳叶刀》发布最新研究,试图量化这一问题的严重程度。
该研究指出,2019年,全球有127万例死亡和抗生素耐药直接相关;约495万人因耐药菌感染病逝。这明显高于此前估计的每年70万AMR相关死亡数。
研究称,AMR是一场“无声的大流行病”,比疟疾、艾滋病(HIV)更致命。
抗生素耐药现状

图1:Global burden of bacterial antimicrobial resistance in 2019:a systematic analysis/THE LANCET
这是全球首次对204个国家和地区抗生素耐药现状的全面评估。研究人员在204个国家和地区、23种病原体、88种病原体-药物组合中,通过分析细菌性AMR所致相关死亡、致残数据,得出以下结论:
2019年,与细菌性AMR相关的死亡人数估计为495万。其中127万死亡可直接归因于细菌性AMR。
从地域看,归因于AMR的全年龄死亡率在撒哈拉以南非洲西部最高,为每10万人死亡27.3人;在澳大拉西亚(位于大洋洲)最低,为每10万人死亡6.5人。
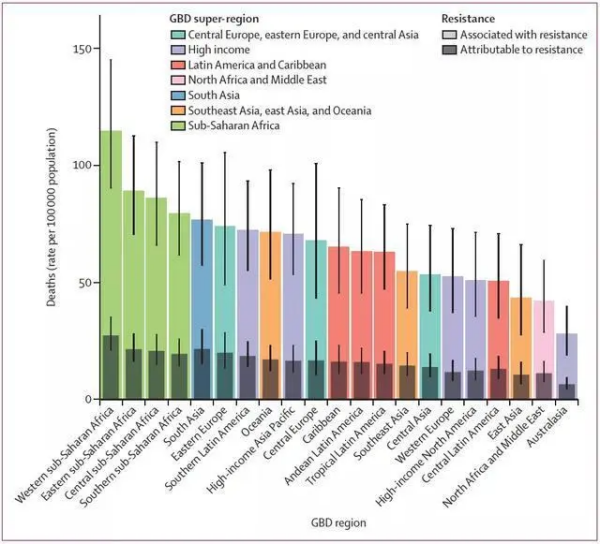
图2:2019年按GBD(全球疾病、伤害和风险因素负担研究)地区划分的可归因于或与AMR相关的所有年龄死亡率。/THE LANCET
2019年,与耐药性相关的下呼吸道感染死亡人数超过150万,是最严重的感染综合征。
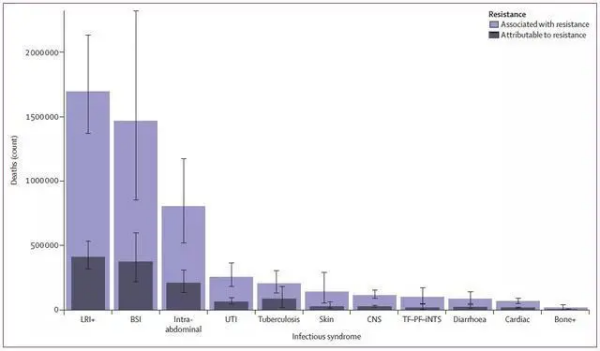
图3:2019年按感染综合征分列的可归因于细菌耐药性和与之相关的全球死亡(计数)。Bone+=骨、关节和相关器官感染;BSI=血液感染;Cardiac =心内膜炎和其他心脏感染;CNS=脑膜炎和其他细菌性脑膜炎感染。Intra-abdominal =腹膜和腹腔内感染;LRI+=下呼吸道感染和胸部所有相关感染;Skin =皮肤和皮下系统的细菌感染。TF–PF–iNTS=伤寒、副伤寒和侵袭性非伤寒沙门氏菌属。UTI=尿路感染和肾盂肾炎。/THE LANCET
与耐药性相关的6大死亡病原体,分别为大肠埃希菌、金黄色葡萄球菌、肺炎克雷伯菌、肺炎链球菌、鲍曼不动杆菌和铜绿假单胞菌。它们导致约92.9万AMR死亡和约3.57亿AMR相关死亡。
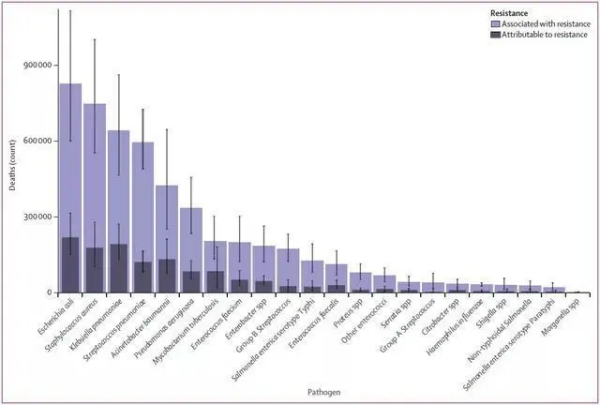
图4:2019年按病原体分列的可归因于和与细菌耐药性相关的全球死亡(计数)/ THE LANCET
2019年,抗甲氧西林金黄色葡萄球菌导致10万多人死于AMR。另有6种病原体-药物组合分别导致5-10万人死亡,它们分别是多重耐药(不包括广泛耐药结核病)、第三代头孢菌素耐药大肠杆菌、碳青霉烯类耐药鲍曼尼菌、耐氟喹诺酮的大肠杆菌、碳青霉烯类抗生素肺炎克雷伯菌和第三代头孢菌素耐药肺炎克雷伯菌。
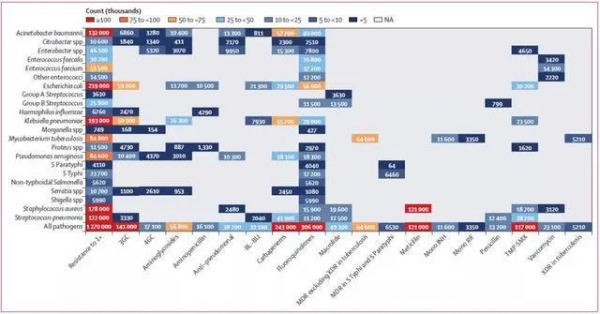
图5:2019年按病原体-药物组合分类的细菌耐药性导致的全球死亡(计数)/THE LANCET
此外,研究者选取7种耐药病原体分离株百分比的原始数据和模型,绘制成地图,以展示不同国家和地区耐药病原体的分布情况。白色区域代表无数据,XDR表示广泛耐药。
耐甲氧西林金黄色葡萄球菌分布情况
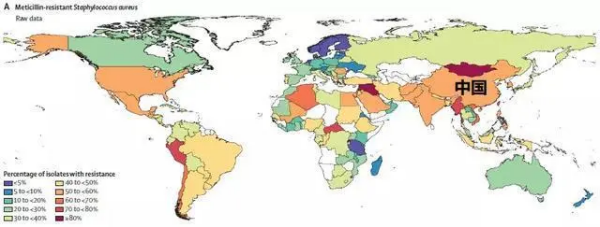
上图是耐甲氧西林金黄色葡萄球菌分布情况。
异烟肼和利福平共耐药(XDR除外)结核分枝杆菌
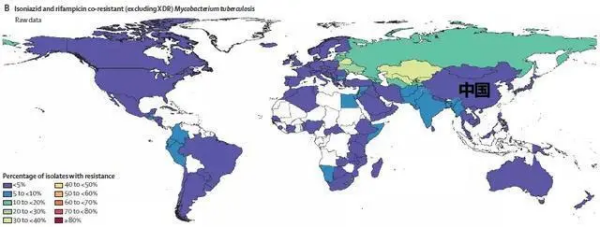
上图为异烟肼和利福平共耐药(XDR除外)结核分枝杆菌的分布情况
第三代抗头孢菌素大肠杆菌
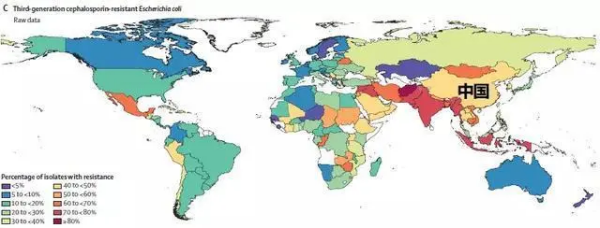
上图为第三代抗头孢菌素大肠杆菌相关情况
耐碳青霉烯类鲍曼不动杆菌
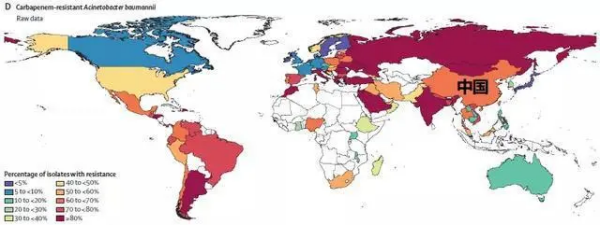
上图为耐碳青霉烯类鲍曼不动杆菌情况
耐氟喹诺酮的大肠杆菌
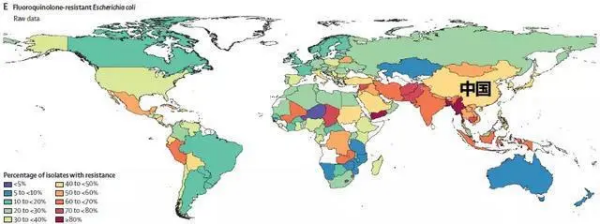
上图为耐氟喹诺酮的大肠杆菌
耐碳青霉烯类肺炎克雷伯菌
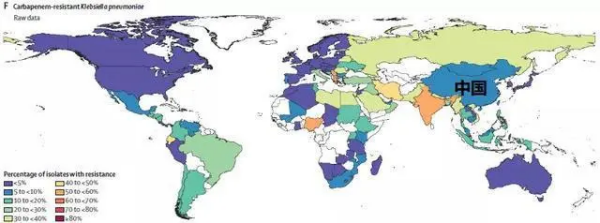
上图为耐碳青霉烯类肺炎克雷伯菌情况
第三代头孢菌素耐药肺炎克雷伯菌
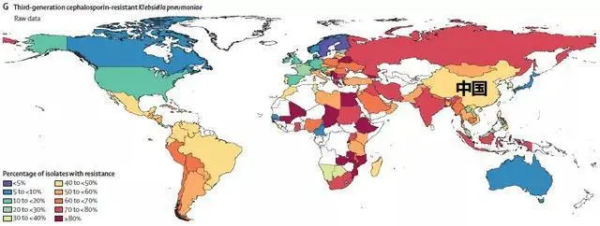
上图为第三代头孢菌素耐药肺炎克雷伯菌的分布情况
根据上述组图总结中国的耐药病原体分布情况,可以发现:
1.耐甲氧西林金黄色葡萄球菌分离比:50%-60%;
2.异烟肼和利福平共耐药(XDR除外)结核分枝杆菌分离比:小于5%;
3.第三代抗头孢菌素大肠杆菌分离比:40%-50%;
4.耐碳青霉烯类鲍曼不动杆菌分离比:60%-70%;
5.耐氟喹诺酮的大肠杆菌分离比:40%-50%;
6.耐碳青霉烯类肺炎克雷伯菌分离比:5%-10%;
7.第三代头孢菌素耐药肺炎克雷伯菌分离比:40%-60%;
概括来说,除异烟肼和利福平共耐药结核分枝杆菌和耐碳青霉烯类肺炎克雷伯菌,其他组合的分离率都在40%以上。其中,耐碳青霉烯类鲍曼不动杆菌分离率最高,达60%-70%。
通过以上研究结果可以看出,如果所有耐药感染被无感染取代,2019年可以避免495万例死亡。如果所有耐药感染被药物敏感感染取代,可以避免127万例死亡。
为此,相关组织和专家提出,应对细菌性AMR挑战的干预策略分为五大类。
第一,预防和控制原则是预防广泛感染的基础,是防治AMR传播的基石。
第二,通过接种疫苗、预防感染,对于减少抗生素需求至关重要。《柳叶刀》配发评论称,目前有6种病原体存在针对性疫苗。其中,接种肺炎链球菌疫苗能有效预防感染。而接种流感病毒、呼吸道合胞病毒、轮状病毒等相关疫苗,能有效缓解病情程度,从而减少不合理用药。
第三,减少接触与治疗人类疾病无关的抗生素使用,是降低风险的重要潜在途径。
第四,当抗生素对改善人类健康(如治疗病毒感染)“非必需”时,应优先减少抗生素使用。
第五,维持对新抗生素开发管道的投资,在无法广泛获得抗生素的地区,尽量使用二线抗生素。
“讽刺的是,抗生素滥用和药物可及性低,往往并存。在撒哈拉以南非洲、南亚和拉丁美洲,AMR相关负担最重。当地耐药菌感染率高,但药物可及性非常低。2/3的AMR相关死亡,都和一线抗生素耐药有关。”《柳叶刀》社论称,目前在研新型抗生素少。很多研究都指出抗生素耐药的紧迫现状,但鲜有研究聚焦于寻找解决方案。
该社论还指出,新冠肺炎大流行可能加剧抗生素耐药问题。大流行期间,患者住院时间延长,抗生素滥用问题加剧。
参考文献
1.Antimicrobial Resistance Collaborators(listed at the end of the paper). Global burden of bacterial antimicrobial resistance in 2019:a systematic analysis. THE LANCET. doi.org/10.1016/S0140-6736(21)02724-0
2.Antimicrobial resistance: time to repurpose the Global Fund. The Lancet. doi.org/10.1016/S0140-6736(22)00091-5
3.The overlooked pandemic of antimicrobial resistance. The Lancet. doi.org/10.1016/S0140-6736(22)00087-3
来源:医学界