近期,生物医药行业几乎都将目光聚焦到了这一事件 —— 美国时间2月10日上午10点至下午3点(北京时间2月11日0点-5点),美国食品药品监督管理局(FDA)肿瘤药物专家委员会(ODAC)将对我国信达生物PD-1信迪利单抗(sintilimab)进行首个美国上市申请(BLA 761222)讨论和审批,适应症为与培美曲塞和铂类化疗联合使用,一线治疗无表皮生长因子受体(EGFR)或间变性淋巴瘤激酶(ALK)基因组肿瘤异常的IIIB、IIIC或IV期非鳞状非小细胞肺癌患者。根据FDA公布的会议议程表显示,美国时间上午10点25分,信达生物将对信迪利单抗的III 期试验ORIENT-11进行有效性和安全性解读。下午1点,FDA ODAC将对信迪利单抗进行讨论。其备受关注的便是仅基于中国地区患者完成的Ⅲ期临床试验ORIENT-11,根据信达为ODAC提供的信迪利单抗全面简介(共81页,全英文,后台回复“信迪利单抗”,获取PDF)显示,截止2021年9月15日,信迪利单抗联合化疗18个月的总生存率(OS)为60.2%,安慰组为43.9%。

ORIENT-11临床数据结果
尽管整个简介中介绍充分,ORIENT-11临床数据具有可靠优势,但在FDA拟定的问题草案中显示,FDA将讨论:ORIENT-11在美国人群以及医疗实践中的推广可及性;能否解决其在美国人群中的临床治疗问题,其可能不适合用于美国医疗实践,是否考虑追加额外的临床试验证明其适用性。
与此同时,FDA公布的另一份关于信迪利单抗审评的简报文件中(共32页,全英文,后台回复“信迪利单抗”,获取PDF),提出了6个质疑性的“关键问题”,并表示ORIENT-11临床试验存在局限性,信迪利单抗缺乏参与国际多中心研究(MRCT)的临床经验。


6个质疑性的“关键问题”
这并不奇怪,过去FDA获批任何一款新药都是基于欧美患者的临床数据,即便是有中国患者参与的全球临床试验,所占的比例也很小。同样的,这些新药在中国申请上市,需要再招募中国患者开展临床研究。确保临床试验中种族和民族多样性,几乎是所有国际制药巨头都确认的原则。对此不难猜测,这场国产PD-1的FDA闯关,要么失败,要么以追加更多临床多中心试验数据宣告推迟延期审评。抛开审评结果,自2020年,国产四款PD-1纳入医保后,过去一年,国内PD-1/L1赛道竞争激烈。截止目前,国内已上市6款国产PD-1,2款进口PD-1;2款进口PD-L1,2款国产PD-L1。
PD-1/L1独特且广谱的抗肿瘤作用机制,决定了其“抢手”的市场前景。据统计,目前国内申报在研的国产PD-1/L1已多达近百种,各具特色,稍微有点“乱花渐欲迷人眼”的意思。
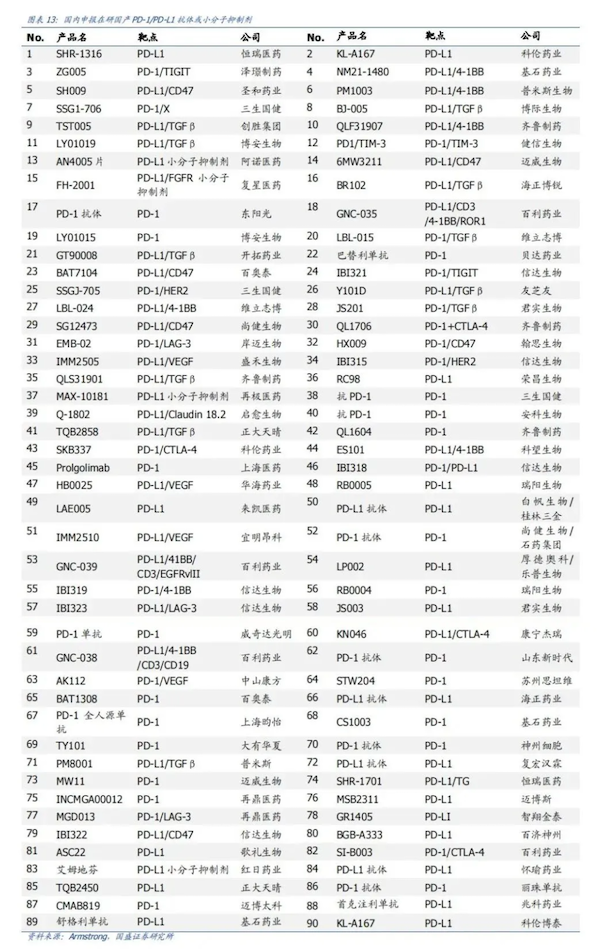
由于国内同质化创新,医保纳入,PD-1内卷焦虑,这导致市场预期大幅降低,倒逼创新药企走出国门,“出海”只是时间问题。
主题:ONC-392:充分发掘CTLA-4未被发掘的潜力时间:2022年2月10日 周四 19:30-20:30毕业于中科院生物物理所,先后在美国希望城贝克曼研究所、清华大学医学院免疫所从事博士后科研工作(T细胞免疫方向)。2018年参与广州昂科免疫生物技术有限公司创建,现任广州昂科免疫总经理。领导团队完成CD24Fc治疗重症新冠肺炎项目在中国的临床申报并获批(该项目最终被默沙东收购)和新一代靶向CTLA-4的创新免疫治疗药物ONC-392(I类新药)在中国的临床申报及临床试验。

广州昂科免疫生物技术有限公司是一家临床阶段的生物制药公司,由知名华人科学家刘阳教授和郑盼教授于2018年创立,公司致力于开发创新免疫治疗药物治疗癌症和自身免疫疾病。公司拥有多个自主研发产品包括一系列免疫检查点相关的一类原创新药的全球权益,并独占许可引进了刘阳教授开发的新一代CTLA-4抗体药物ONC-392和另一系列first in class产品ONC-78X的大中华区权益。ONC-392将于2022一季度在中国结束I期临床试验,由美国OncoC4 Inc申办的ONC-392 I期临床研究于2021年底发布的临床试验结果验证了刘阳教授提出的全新靶向CTLA-4肿瘤免疫治疗理论,也奠定了ONC-392在该领域的全球领先地位。广州昂科免疫自研的全球首创靶向CD24-Siglec通路用于重症新冠肺炎等炎症性疾病的免疫调节产品AI-071将于2022年进入临床开发阶段。











