《“健康中国2030”规划纲要》提出,到2030年我国主要健康指标进入高收入国家行列,其中“干细胞与再生医学”作为重大科技项目被列入规划纲要,旨在推进医学科技进步,推动健康科技创新。《战略性新兴产业重点产品和服务指导目录》,支持包括干细胞在内的细胞治疗产品等领域的生物产业发展。
干细胞像是生命的种子,在一定条件下,可以分化成多种功能细胞,具有修复各种组织功能和再生器官的能力,被医学界称为“万能细胞”。
“未来5至10年,干细胞技术在医学上的应用会出现颠覆性革命。”东方医院院长刘中民深刻感觉到:近年来,化学药物、外科手术等传统医疗手段已越来越受到人口老化、慢性病及肿瘤高发的挑战,以干细胞、免疫细胞治疗等为代表的细胞治疗新技术发展迅猛,已成为当今世界生物医药领域研发的热点。未来5年全球范围将有更多干细胞药物获批上市。
裴钢,原同济大学校长、中科院院士,国内干细胞领域带头人,一次次强调,“要拿出传教的精神来宣传干细胞。”
2021年12月12日,中科院院士、中国细胞生物学学会干细胞生物学分会会长季维智在中国干细胞第十一届年会上明确指出:中国在干细胞领域的研究,毋庸置疑位于世界第一梯队。

随着全球细胞与基因治疗产业迈入了高速发展期,当前全球已登记的细胞与基因治疗相关临床试验已超过7000余项,其中近3000项已完成临床试验研究,并进行了数万例干细胞移植。
国内干细胞药物注册也正处在蓬勃发展的趋势中,自从2018年国家药品监督管理局药品审评中心(CED)重新受理干细胞新药临床试验申报以来,干细胞药物临床试验的申请稳步增长。就承办受理号总量,从2018年申报5个(以受理号计)增长至2022年的26个,较2021年度增长了一倍,我国干细胞新药研发速度明显加快。

△2018-2022年干细胞药品申报一览
申报情况
2022年CDE受理干细胞药物临床申请26项(以受理号计),其中国产1类创新药注册申请25项,进口1类创新药注册申请1项。进口干细胞药物为Cytopeutics脐带间充质干细胞(Neuroncell-EX)。
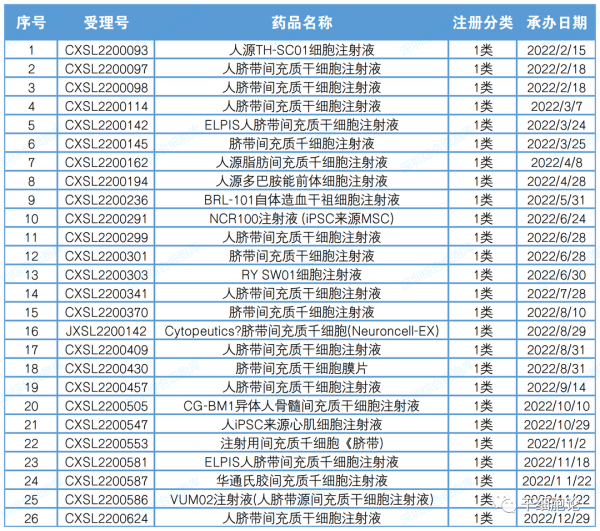
△2022年度干细胞药物注册申请受理清单
临床试验默示许可情况
2022年CDE合计默许许可11款干细胞药物的16项临床试验。其中使用间充质干细胞的有11项,间充质干细胞使用类型占比达到68%。(相关阅读:行业动态:2022年国内干细胞药物IND获批情况汇总)
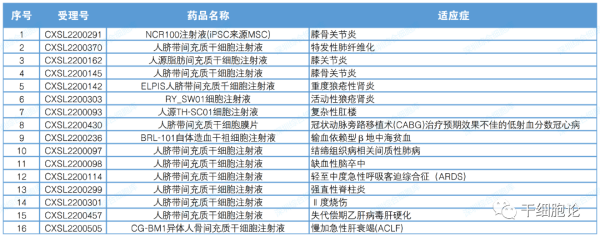
△表3 2022年度干细胞药物临床默示许可一览表
干细胞的双轨制管理
目前,我国干细胞(造血干细胞除外)是按药品(生物制剂)和技术(医疗技术)实行“双轨制”监管。

企业的干细胞制剂按药品申报,由国家药品监督管理局监管;医疗机构开展的干细胞技术临床研究,由国家卫生健康委员会监管。
双轨制之药品路线
2018年,国家药品监督管理局药品审评中心开始重新受理干细胞新药临床试验( IND )注册申请,伴随着临床试验默许制的落地,干细胞新药研发速度明显加快,干细胞IND数量稳步增长。
截至2023年6月30日,在国家药品监督管理局药品审评中心查询到的通过临床试验默示许可的干细胞药品共65种,与干细胞临床研究备案项目一样,适应症覆盖多系统疾病。
干细胞疗法前景可期
干细胞技术一直以来被视为“再生医学技术”,被誉为继药物治疗和手术治疗之后的第三次医学革命,是近年来国际医学前沿重点发展领域。它为传统医学难以根治的各类疑难杂症提供了一条新的治愈途径。
根据全球最大临床试验登记网站上的信息,诸如新冠感染后遗症、糖尿病、骨髓增生异常综合征、新生儿严重缺氧缺血性脑病、阴茎硬结症、勃起功能障碍等疾病的临床治疗研究也在应用干细胞开展治疗。
目前世界范围内陆续有干细胞药物获批上市,我国国内干细胞临床试验发展势头也很强劲,同时国家和地方政策频出,指导行业有序、高质发展,相信随着干细胞技术在疾病领域的不断突破,其成果将惠及更多人群。