10月26日,动物医学院刘天龙副教授课题组在期刊《新兴微生物与感染》(Emerging Microbes & Infections)在线发表了研究论文,题为“HEV感染导致的胎盘滋养层细胞自噬抑制可能在不良妊娠中发挥重要作用”(Vital role of Autophagy flux inhibition of placental trophoblast cells in pregnancy disorders induced by HEV infection)。研究以自噬作为切入点,揭示了戊型肝炎病毒(HEV)感染引起流产、早产等不良妊娠的潜在分子机制。
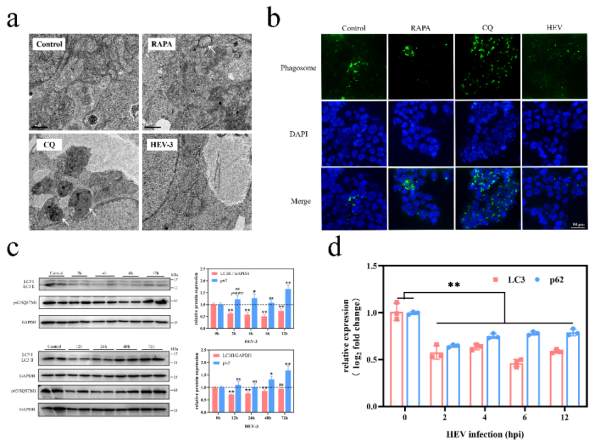
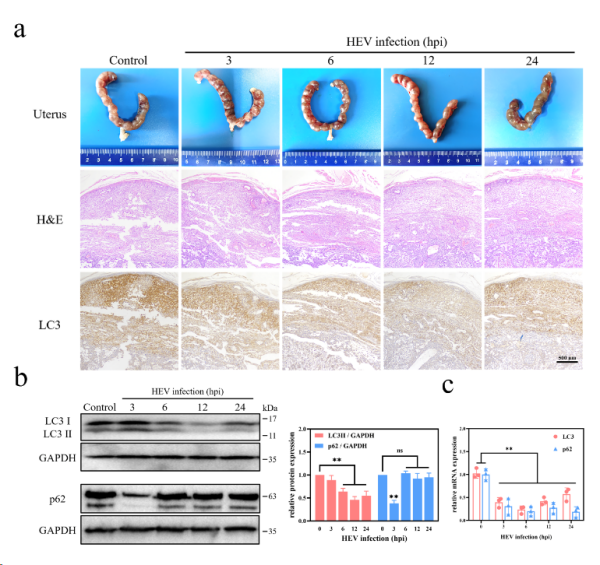
HEV是人畜共患的重要病原之一,威胁全球公共卫生并在我国广泛流行。一般群体感染HEV多可自愈,但对部分患者如免疫不全、孕妇及老年患者具有严重危害。人或动物在妊娠状态下感染HEV出现明显的垂直传播、早产、流产、胎儿发育不良等问题,对人类健康及畜牧动物经济造成多重影响。自噬是机体一种必要的清除机制,广泛存在于真核细胞中。生理功能包括提供能量、维持细胞稳态、促进异常细胞凋亡等。妊娠过程中,自噬在滋养层细胞的增殖、分化、侵袭和血管重塑中起着重要作用,细胞自噬的异常可能引起胎盘功能损伤,导致不良妊娠结局。该研究首先构建了妊娠ICR小鼠感染HEV的动物模型,并导致母鼠产仔率显著下降,出现明显的子宫内流产,流产率为24.19%。收集病毒感染后的体外滋养层细胞(JEG-3),在电镜及荧光显微镜下进行观察。结果发现自噬泡数量显著减少,细胞内自噬标志蛋白LC3表达降低,p62蛋白蓄积,表明HEV感染导致JEG-3细胞出现明显的自噬抑制。小鼠胎盘组织中也呈现类似结果。HEV急性感染后,胎盘组织内LC3蛋白量显著降低,LC3及p62转录受到抑制。本研究以自噬作为切入点,以滋养层细胞和胎盘组织为研究载体,揭示了HEV感染导致不良妊娠的潜在致病机制,为防治妊娠期感染HEV提供新思路。后续工作正围绕纯化病毒蛋白的致病机制及自噬上游调控位点展开深入研究,并将进一步探索病毒感染与胎儿发育不良、生长迟缓之间的关系,为人与动物健康的持续发展贡献力量。中国农业大学动物医学院博士研究生杨忆斐为第一作者,刘天龙副教授为本文的通讯作者。本研究工作受国家自然科学基金项目(31802162)、北京市自然科学基金项目(6202017、6222022)资助。