8月16日,百济神州在ClinicalTrials.gov登记了靶向BTK的降解剂BGB-16673,适应症包括B细胞淋巴瘤、边缘区淋巴瘤滤泡性淋巴瘤等,这是百济神州首个启动临床的PROTAC项目。PROTAC(Proteolysis-targeting chimera)全称蛋白降解靶向嵌合体,即利用泛素-蛋白酶体系统诱导靶向蛋白降解。近年来,PROTAC技术日臻成熟,未来有望突破不可成药的难题,并克服由于靶标突变或过表达带来的耐药性问题。
PROTAC概念
自从人类基因组被解读以来,研究人员便试图靶向成千上万导致疾病的蛋白。但目前仅有20%的蛋白能用小分子或大分子药物调控,高达80%的蛋白无法被现有药物调控。此外,由于小分子和抗体药物均需要持续占据靶蛋白活性位点以阻断其功能,因此需要达到足够高的浓度方可发挥作用,这种作用机制不可避免带来耐药性或不可成药等问题。PROTAC技术是药物研发的新兴方向,与传统药物阻断蛋白的模式不同,PROTAC通过两种配体与靶蛋白与泛素E3连接酶同时结合,形成稳定的靶蛋白-PROTAC-E3连接酶三元复合物,诱导泛素化并由蛋白酶体降解,有望突破不可成药的蛋白靶标。
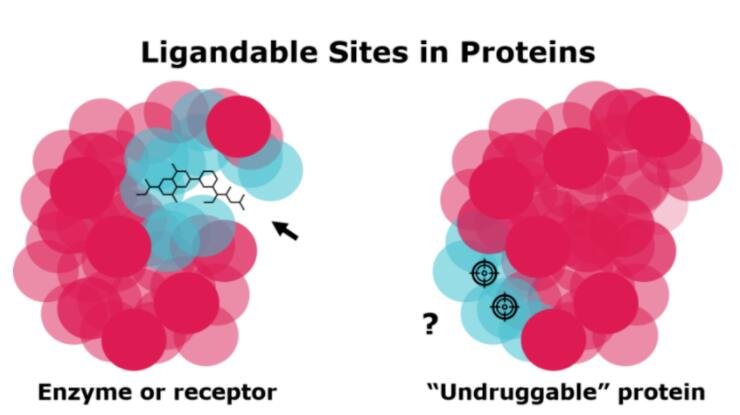
PROTAC的技术源头与泛素调节的蛋白降解关系密切。泛素是一种存在于所有真核生物中的小蛋白,由76个氨基酸组成,分子量大约为8.45kDa。泛素的主要功能是标记需要分解的蛋白质,当泛素连接到蛋白上后,会导致这些蛋白被运送到蛋白酶体中进行降解,实现细胞内蛋白的平衡。总的来说,泛素参与了细胞周期、增殖、凋亡、分化、转移、基因表达、转录调节、信号传递、损伤修复、炎症免疫等几乎一切生命活动的调控。
蛋白质泛素化作用是后翻译修饰的一种常见形式,该过程能够调节不同细胞途径中各式各样的蛋白质底物。蛋白质泛素化是一种ATP依赖的酶促反应,其降解过程须通过三种酶逐步催化,包括E1泛素激活酶、E2泛素结合酶和E3泛素连接酶(E3 ligase)。具体而言,首先,E1水解ATP成功将泛素分子腺苷酸化,泛素转移到E1的半胱氨酸残基上;其次被腺苷酸化的泛素分子转移到E2的半胱氨酸残基上;然后,E3识别需要被降解的靶蛋白,并催化泛素分子从E2上转移至靶蛋白上;最终26S蛋白酶体识别并降解连续被四个及以上泛素化的靶蛋白。
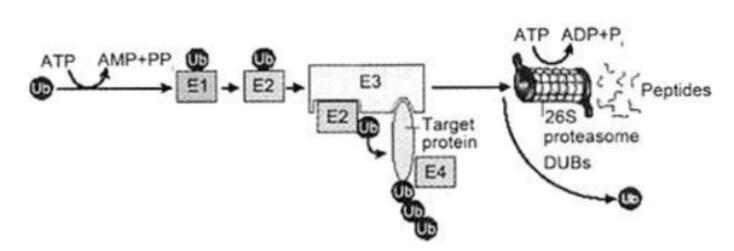
图:蛋白质泛素化示意图
PROTAC的结构:小分子PROTAC一般由三部分组成:目标蛋白(Protein of interest, POI)配体、E3泛素连接酶配体及连接体Linker。当PROTAC分子进入细胞后,其结构中的目标蛋白配体可特异性地与相应的靶蛋白结合,而另一端可以募集E3连接酶从而形成POI-PROTAC-E3 ligase三元复合物,其中E3连接酶可介导泛素结合酶E2对POI泛素化。三元复合物解离后,被泛素“标记”的POI被蛋白酶体识别并降解从而选择性降低靶蛋白的水平。
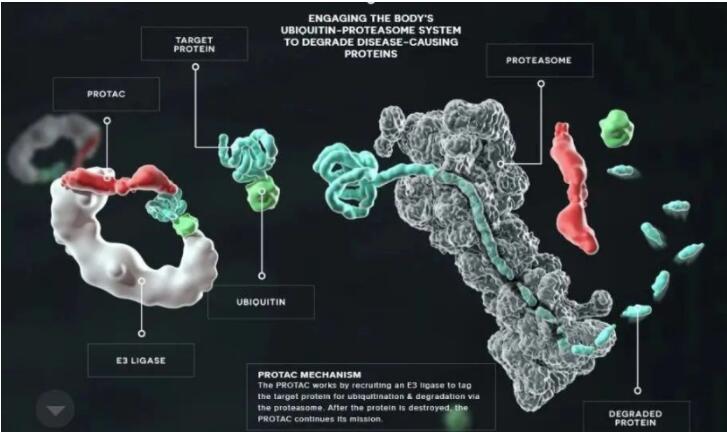
图:PROTAC作用机制示意图
理论上,PROTAC仅提供结合活性,无需直接抑制目标蛋白的功能活性,通常认为是事件驱动,即“Event-driven”,而非传统的占有驱动“Occupancy driven”。其优点主要包括靶向不可成药蛋白、克服耐药性问题、药物剂量较低等。
第一,靶向不可成药蛋白,克服耐药性问题。PROTAC既可有效靶向目标蛋白,又可以将其降解清除。与传统小分子药物不同,PROTAC无需与目标蛋白长时间和高强度的结合,便可捕获蛋白并将其降解,因此有望突破传统难以成药的靶点并克服耐药性问题。
第二,药物剂量较低。PROTAC的反应过程类似催化反应,药物可重复利用,裂解目标蛋白,并不需要等摩尔量的药物,药物的剂量有望降低。
但PROTAC开发难度较大,目前在研的PROTAC存在口服吸收及过膜性较差等问题。一方面,PROTAC药物属于双靶点药物,分子量较大,结构复杂,药代动力学并不乐观,口服吸收和过膜性存在挑战;另一方面,PROTAC靶标蛋白降解能力显著,但由于靶蛋白在正常细胞中也会表达,PROTAC对正常组织的毒性须密切关注。此外,用于小分子药物早期筛选的Lipinski的“无法则”并不适应于PROTAC领域,
Protac先锋企业:Arvinas
Arvinas是全球PROTAC技术的新锐公司,旨在利用人体自身的天然蛋白处理系统选择性高效降解和去除引起疾病的蛋白。目前,公司已有两款PROTAC药物进入临床Ⅱ期,分别是靶向雄激素受体(AR)的ARV-110和靶向雌激素受体(ER)的ARV-471。
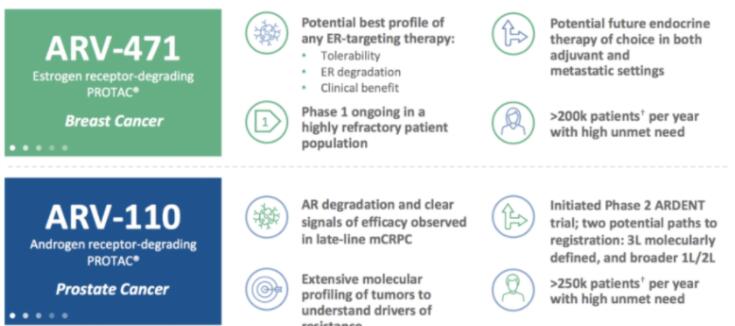
(1)ARV-110是一款选择性靶向AR的PROTAC小分子药物,用于转移性去势抵抗前列腺癌(mCRPC),目前处于临床Ⅱ期。与恩杂鲁胺和阿比特龙抑制AR不同,ARV-110直接将雄激素受体摧毁,有望提升传统“占有”机制的疗效。此外,ARV-110可降解目标蛋白的复制,因此有望克服目标蛋白的过表达和突变,目标蛋白的过表达和突变是SOC耐药的重要原因。
在2020年ASCO上,Arvinas公布了ARV-110的Ⅰ期临床数据,试验纳入18名先前接受过至少2线治疗的mCRPC患者,包括恩杂鲁胺和阿比特龙。截至2020年1月,在140mg组中,25%(2/8)患者的PSA水平下降50%,其中一名患者出现肿瘤的缩小,证实了ARV-110具有抗前列腺癌的活性。安全性方面,ARV-110整体安全性良好,但有2名患者同时服用瑞舒伐他汀时出现3/4级DLT和AST/ALT升高,因此,在后续的研究中,两种药物应避免同时服用。
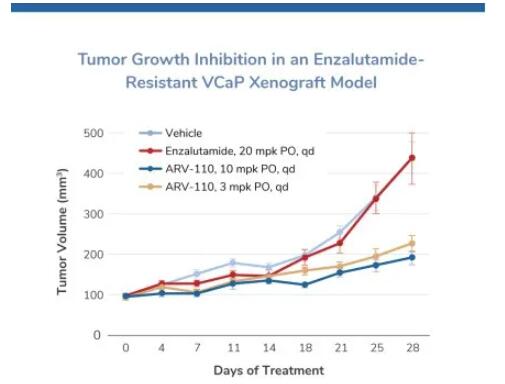
图:ARV-110对恩杂鲁胺耐药的前列腺癌具有潜在疗效(数据来源:Arvinas)
(2)ARV-471靶向雌激素受体(ER),适应症为局部晚期或转移性ER阳性/HER2阴性乳腺癌,目前处于Ⅱ期剂量扩增临床试验。尽管来曲唑、氟维司群等雌激素受体抑制剂在乳腺癌治疗中取得了一定的成功,但由于耐药性的存在,许多患者出现疾病进展。ARV-471利用PROTAC技术降解ER蛋白,有望达到治疗ER+乳腺癌的目的。
在2020年AACR上,Arvinas公布了ARV-471的Ⅰ期中期试验结果,针对平均接受过5种前期疗法ER+、HER2-乳腺癌患者,ARV-471可显著降低肿瘤患者组织中的ER表达水平,平均将ER水平降低62%,最多降低90%。在14例可评估的患者中,一例实现确认的部分缓解,2例达到未确认的部分缓解。安全性方面,未发生3-4级不良事件和DLT。
7月22日,Arvinas与辉瑞宣布将共同开发和商业化ARV-471。根据协议,Arvinas将获得6.5亿美元的预付款及高达14亿美元的里程碑付款。众所周知,辉瑞的CDK4/6抑制剂哌柏西利正面临礼来阿贝西利的冲击,继哌柏西利与来曲唑/氟维司群等药物联用方案后,与ARV-471的联用或是哌柏西利巩固市场份额的新思路,ARV-471与哌柏西利的联用方案目前处于Ⅰb期。
图:ARV-471结构

国内已有一批企业相继布局PROTAC技术,包括开拓药业、海思科、百济神州、成都分迪科技、上海和径药业、海创药业、凌科药业等,其中,临床进展居前的PROTAC药物包括海思科的HSK29116和开拓药业的GT20029。
海思科的HSK29116是基于公司的PROTAC研发平台筛选出的口服BTK-PROTAC小分子抗肿瘤药物,一方面可通过特异性结合BTK直接抑制BKT活性;另一方面能诱导BTK泛素化标记,通过蛋白酶体途径将其降解,从而阻断BCR信号通路的传递,抑制B细胞淋巴瘤细胞的生长和增殖,发挥双重抗肿瘤作用。2021年4月,HSK29116已启动国际多中心Ⅰ期临床,计划在中国入组86人,国际入组126人。
开拓药业的GT20029是一种降解AR蛋白的AR降解剂,适应症为雄激素性脱发及痤疮。GT20029的作用机制为将AR蛋白招募至E3泛素连接酶进行降解,当其作用于表层皮肤的局部组织及局部皮囊皮脂腺,可降低AR对雄激素的敏感性,而无需全身接触药物。根据动物试验,GT20029的有效性优于其他小分子AR抑制剂,且不会引起过度药物蓄积及明显的副作用。2021年7月28日,GT20029Ⅰ期临床试验完成首批受试者给药。