
对于角质形成细胞在分化的各个阶段的基因表达的了解已经取得了很大的进展,并且已经知道了一些相关的信号通路。角质形成细胞的整体分化过程遵循基底细胞中非常活跃的整体转录梯度,而在进一步分化的细胞中,转录谱越来越受限。越来越多的证据表明,表观遗传过程如DNA甲基化和组蛋白修饰在角质形成细胞分化过程中转录逐渐沉默中发挥重要作用。
具有表皮正常分化遗传性缺陷的自发性动物突变体为进一步确定建立特定基因表达模式所需的复杂调控网络的组成部分提供了机会。由于其特殊的群体结构,纯种犬特别适合进行基因分析。利用犬遗传学进行皮肤研究的成功例子包括:与毛发特征决定相关的基因,外胚层发育,一种鱼鳞病,先天性干燥性角结膜炎和鱼鳞病样皮肤病,以及中国沙皮犬皮肤过度折叠有关的基因。
遗传性鼻角化不全(HNPK)是一种单基因常染色体隐性遗传性皮肤病,可导致拉布拉多犬鼻平面上的结痂和裂隙。研究者进行了全基因组关联研究(GWAS),并将致病突变定位于2号染色体上的一个小区间。重新排序了影响犬HNPK的整个基因组,发现三个蛋白质突变临界区间。在更大的犬群中对这三个变异体进行了基因分型,只有一个变异体显示出完美的基因型-表型关联,这促使我们认为这一变异体(SUV39H2的错义突变)是最有可能导致HNPK的变异体。SUV39H2酶参与组蛋白甲基化和表观遗传沉默,一个过程确定角化细胞分化过程中基因表达的调控。预计SUV39H2功能缺失将导致分化延迟,这与在患HNPK的拉布拉多犬的鼻部活检中观察到的组织病理学变化一致。因此,我们的结果提供了犬类中最有可能的遗传性疾病致病突变,这些突变现在可以通过选择性育种来根除。此外,研究结果也提供了SUV39H2可能参与角质形成细胞分化的第一个线索,其在体内的功能尚不完全清楚。
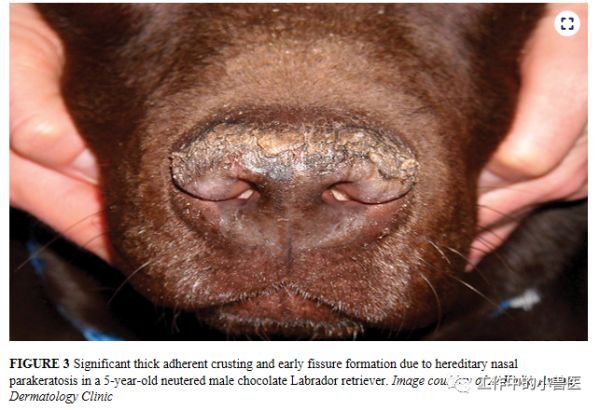
https://www.cliniciansbrief.com/article/nasal-planum-disease-dogs
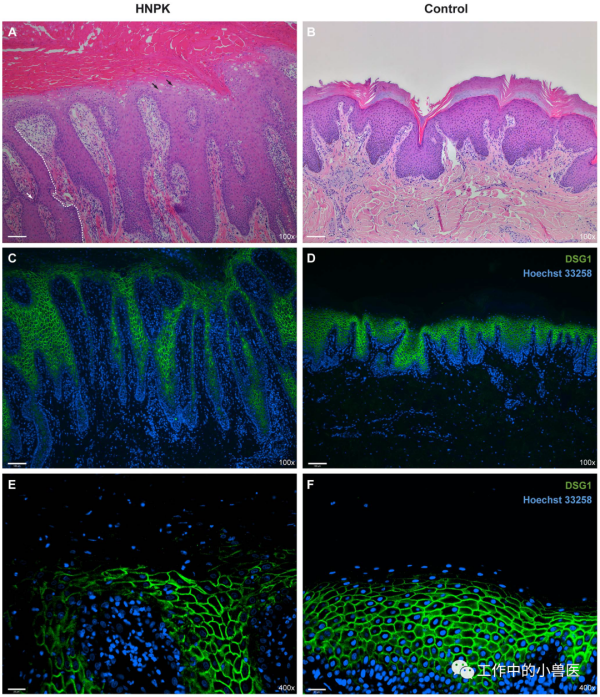
图3 患HNPK和未患HNPK的拉布拉多猎犬的鼻平面组织。(A)一只HNPK患犬的苏木精-伊红染色显示,弥漫性角化不全性角化过度,表皮上层角质形成细胞水肿(黑色箭头),表皮淋巴细胞胞吐,血管周围真皮淋巴细胞浸润。在患病犬中形成细长的,有时融合的纤细网状表皮突,导致表皮增厚(一个表皮突的边界用白色虚线表示,一个融合线用白色箭头表示)。(B)对照犬HE染色。(C-F)桥粒芯糖蛋白1 (DSG1,绿色)在两种不同放大倍数下的免疫检测。细胞核用Hoechst 33258反染(蓝色)。DSG1染色模式在HNPK组和对照组之间没有明显的差异。Scale bar=100 mm for HE/DSG1 100×,25 mm for DSG1 400×
在拉布拉多猎犬中,HNPK的临床症状仅局限于鼻扁平的表皮。目前尚不清楚为什么广泛表达的组蛋白修饰酶的缺陷会导致非常组织特异性的临床表型。推测,这可能是由于部分冗余的H3K9甲基转移酶的组织特异性表达谱,而鼻平面的表皮是SUV39H2缺失无法得到补偿的唯一组织。尽管如此,在这一点上也无法解释为什么Suv39h2缺陷小鼠没有表现出类似的表型。但可以解释为,小鼠的鼻平面是非常小的,细微的变化是很难评估的。
形态学分析清楚地表明,HNPK表型不是由于角质形成细胞的过度增殖。因此,HNPK表型似乎很有可能是由终末角质形成细胞分化的改变引起的。分化标志物DSG1在病例犬和对照犬中相似的表达模式进一步证明,这种分化延迟可能主要局限于表皮的最外层。SUV39H2是一种染色质修饰酶,是参与细胞分化调控的合理候选酶。虽然还没有完整的功能证据来证明它在角质形成细胞分化中的作用,但实验结果的基因数据和详细的体内组织病理学分析强烈表明,SUV39H2:p.N324K在角质形成细胞分化中的作用,其缺陷是HNPK的致病原因。进一步的分化标志物和RNA-seq实验将有助于阐明SUV39H2缺陷细胞中染色质修饰缺失导致角质形成细胞分化过程受损的下游效应分子发生了改变。