礼蓝(四川)动物保健有限公司
结膜吸吮线虫(旋尾目,吸吮科),已被证实是一种会感染家养动物(犬和猫)、野生动物(如狐狸、兔子)和人类眼部的病原体。在过去的二十年,一些欧洲国家有越来越多的此类寄生虫感染的报道。眼线虫成虫和幼虫的感染症状从轻微(如流泪、眼部有分泌物、溢泪)到严重(如结膜炎、角膜炎和角膜混浊或溃疡)。本试验评估10%吡虫啉和2.5%莫昔克丁滴剂(Advocate®, Bayer Animal Health)的临床疗效和安全性,用米尔贝肟/吡喹酮片(Milbemax®, Novartis-Animal Health)作为阳性对照组,同时治疗自然感染结膜吸吮线虫的犬,第三组未经治疗作为空白对照组。在意大利南部的一个眼线虫流行区域,选择了47只犬(27只雌性犬,20只雄性犬),其中一只犬的眼部至少有一只结膜吸吮眼线虫成虫。每只犬记录体重,然后按照治疗计划进行随机分组(G1组为10%吡虫啉和2.5%莫昔克丁滴剂治疗组,G2组为没有任何治疗的空白对照组,G3组为米尔贝肟/吡喹酮片治疗组)。分别在第7天、14天、28天和35天对每只犬进行体格检查,对双眼进行检查来评估感染程度,包括结膜穹窿和第三眼睑的结膜吸吮眼线虫成虫计数和临床评分。G1组的犬在D0天和D28天给药治疗,G3组的犬在D0天和D7天给药治疗。G1组在治疗后每次检查结果的有效率均为100%(p < 0.01),而G3每次检查后的有效率分别是D7天为57.39%(p < 0.05),D14天有效率为92.79%,D28天和D35天有效率为100% (p < 0.01)。使用10%吡虫啉和2.5%莫昔克丁滴剂治疗结膜吸吮线虫引起的犬眼线虫病有明显的治疗效果。目前,鉴于在欧洲允许广泛使用Advocate®治疗犬寄生虫感染,所以可以推荐使用此配方治疗犬结膜吸吮眼线虫感染。
关键词:眼线虫;结膜吸吮线虫;Advocate®
引言
自从在意大利北部首次诊断出犬感染结膜吸吮眼线虫(旋尾目,吸吮科)[1],在其他一些欧洲国家如意大利、比利时、法国、希腊、葡萄牙、西班牙和瑞士有越来越多此类寄生虫感染的报道[2]。在欧洲,结膜吸吮线虫已被证实是一种会感染家养动物(狗和猫)、野生动物(如狐狸、野兔、家兔)眼部的病原体[3]。最近,生活在东欧国家的犬、猫和狐狸感染眼线虫的病例数量激增。由于这种线虫以前分布在东亚国家(如中国、泰国、日本等),所以被称为“东方眼线虫”,也被认为是感染人类的一种病原体。然而,由于欧洲国家的大量报道,“东方眼线虫”这个名称已不再合适。
在欧洲的意大利[4]、西班牙[5]、克罗地亚[6]和塞尔维亚[7]都报告了人类眼线虫病例,同时也证实这些国家的动物也感染有眼线虫。在欧洲动物和人类眼线虫感染的数量增加与变色绕眼果蝇(双翅目,果蝇科,果蝇亚科)的存在有关,它是结膜吸吮眼线虫的中间宿主[8],主要以被感染动物的泪腺分泌物为食。
眼线虫成虫和幼虫感染的症状从轻微(如流泪、眼部有分泌物、溢泪)到严重(如结膜炎、角膜炎和角膜混浊或溃疡),感染症状轻重也与眼部内的寄生虫多少有关[9]。可以用生理盐水冲洗结膜囊的形式移除眼线虫的成虫和幼虫,成虫也可以用镊子或拭子收集。
局部滴注有机磷酸酯类可以成功治疗眼线虫感染[10],1%的莫昔克丁也可以有效杀死结膜吸吮眼线虫[11]。尽管如此,局部给药是一种说明书外的使用方式,可能会刺激眼部组织,因此在兽医实践中是不被接受。此外,米尔贝肟/吡喹酮片剂(Milbemax®, Novartis-Animal Health),米尔贝肟最小含量0.5mg/kg,已被证实可以显著降低犬猫眼线虫的自然感染率[12],并且这是迄今为止欧洲唯一注册的可以用于治疗犬眼线虫病的产品。与此同时,10%吡虫啉和2.5%莫昔克丁滴剂被证实了治疗和预防犬眼线虫的有效性[13]。
本试验的目的是评价10%吡虫啉和2.5%莫昔克丁治疗自然感染的犬眼线虫病的临床疗效和安全性,用米尔贝肟/吡喹酮片治疗作为阳性对照组。
材料与方法
意大利南部的巴西利卡塔地区是结膜吸吮眼线虫流行区域,对此区域的私人饲养的犬只进行了实地研究实验,本试验采用GCP阴性对照、阳性对照和盲法试验方式进行。进行试验的动物生活区域已经有眼线虫感染的相关病例报道[14]。试验选择了47只不同品种的犬(27只雌性犬,20只雄性犬),年龄从7个月到13岁不等,健康状况良好且眼部至少有一只活的结膜吸吮眼线虫成虫(图1)。收集宠主知情同意书。试验犬的详细资料见表1。

图1 一只犬的眼睛感染了结膜吸吮眼线虫
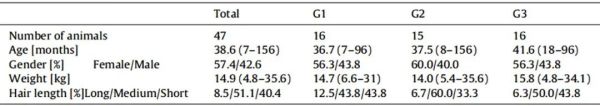
表1 试验犬的数据
试验D0天对试验动物进行物理检查和双眼检查,包括第三眼睑下的检查以便发现结膜吸吮线虫并计数。记录眼线虫感染的临床症状,如流泪、结膜炎、眼部有分泌物、角膜炎和溃疡,并分为无症状、轻度、中度或重度。每只犬记录体重,然后按照治疗计划进行随机分组(G1组为10%吡虫啉和2.5%莫昔克丁滴剂治疗组,G2组为没有任何治疗的空白对照组,G3组为米尔贝肟/吡喹酮片治疗组)。两种产品均按照说明书使用。特别注意,Advocate®包含2.5 mg莫昔克丁和10 mg吡虫啉/kg,Milbemax®包含0.5 mg/kg米尔贝肟和5 mg/kg吡喹酮。
分别在第7天、14天、28天和35天对每只犬进行体格检查,对双眼进行检查来评估感染程度,包括结膜穹窿和第三眼睑的结膜吸吮眼线虫成虫计数和临床评分。在D7,根据米贝肟/吡喹酮片产品说明书对G3组中的犬进行第二次治疗。在D28,G1组的犬进行了10%吡虫啉和2.5%莫昔克丁滴剂的第二次治疗。在D35试验结束,用5 mL(0.9%)生理盐水冲洗结膜囊收集样本,并保存在无菌管中,评估是否存在结膜吸吮眼线虫幼虫。随后摘除结膜吸吮眼线虫成虫。试管在700g下离心5 min。吸去上清液,在光学显微镜(40×)下分析沉积物(1 mL溶液)中的幼虫计数。对眼线虫的幼虫和成虫进行形态学鉴定[15]。
从D0到D35,主人每天观察所有的试验犬,评估和记录健康状况,如果出现异常,兽医负责检查并记录犬临床检查结果。
统计分析
样本量是基于与未治疗的对照组相比,10%的吡虫啉和2.5%的莫昔克丁具有减少犬的结膜吸吮眼线虫成虫百分比方面的优势。根据治疗组未感染犬的预期患病率为90.47%[16],未治疗对照组的预期患病率为23.8%,每组最小样本量为10只犬[17],置信区间为95%,统计效能为90%。为了解决中间有退出者,每组的试验动物数量定为15只。
根据治疗计划,试验犬被随机分组,每组有三只患病犬。每组的患犬被随机分配到三个试验组中,疗效评价主要是通过对比G1、G2,评估在D7、D14、D28、D35时完全消除犬眼线虫成虫的数量。此外,作为次要的描述参数,记录G3组的治疗效果、眼线虫的数量、严重程度以及眼部是否存在临床症状,在D7、D14、D28、D35时与未治疗组进行比较。采用以下公式计算每个时间点对结膜吸吮眼线虫感染的治疗效果(%):
疗效=[(未治疗组阳性的%−治疗组阳性的%)/未治疗组中阳性动物的%] × 100
如果G1组或G3组与未治疗对照组(G2)之间存在显著差异,则表示有效,通过Fisher测试法精确计算得到5%的显著差异具有统计学意义。
在每个时间点治疗组与对照组比较,眼线虫数量及眼部的临床症状,治疗效果表述方式如下:
减少率%[t] = (Ct0–Ct)/Ct0) × 100,Ct0为治疗的计数,Ct为治疗后每个时间点的计数。采用标准统计假设,用方差分析法分析治疗后犬的眼线虫数量减少的显著性。
按照当前的指导原则进行统计学分析[18]。
结果
各试验组中,犬只感染结膜吸吮眼线虫的程度和表现的临床症状的占比都是相同的(p < 0.05)。表2记录了试验的每个时间点呈阳性犬的数量和百分比。G1组(10%吡虫啉和2.5%莫昔克丁)在治疗后每个时间点的有效率均为100%(p<0.01)。G3组(米尔贝肟/吡喹酮片)在D7的有效率为57.39%(p<0.05),在D14的有效率为92.79%,在D28和D35的有效率为100%(p<0.01)。G1组和G3组在D7时的疗效有显著差异(p < 0.05),但其他时间点的疗效没有显著差异。双眼中活的结膜吸吮眼线虫成虫总数和平均值见表3。在D7时G1组(吡虫啉10%,莫昔克丁2.5%)的双眼寄生虫数量已经减少了100%,而G3组(米尔贝肟/吡喹酮片)在D7时双眼寄生虫数量减少90.91%,在D14时为97.73%,D28和D35时减少100%。对照组G2的双眼寄生虫数量也有自然的轻度下降(在D7、14、D28和D35时寄生虫减少率分别为29.31%、24.14%、34.48%和18.97%)。在治疗后的所有时间点,G1组和G3组与对照组的平均虫体数量均有显著差异(p < 0.01)。

表2 试验犬结膜吸吮眼线虫成虫感染阳性的数量和百分比
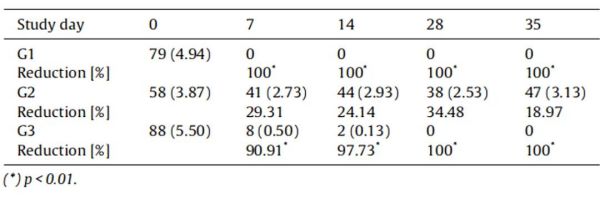
表3 双眼中结膜吸吮眼线虫成虫数量(和平均值)
结膜吸吮眼线虫感染眼部后的临床症状包括流泪、眼部有分泌物、结膜炎等。在D7时,除了G3组中有一只犬表现出角膜溃疡或结膜炎,其他试验犬只均没有以上症状。由于不同眼部症状的发生率低,仅对流泪和结膜炎进行了统计分析。G1组(吡虫啉10%,莫昔克丁2.5%)和G3组(米尔贝肟/吡喹酮片)的治疗没有发现不良反应,与对照组相比,只有在D28时G2组和G3组左眼的结膜炎症状有显著性差异。
讨论
使用吡虫啉10%和莫昔克丁2.5%滴剂治疗犬眼线虫有很好的效果。与米尔贝肟/吡喹酮片(Milbemax®)相比,该配方治疗眼线虫病更有效。事实上,在第一次治疗后没有检测到眼线虫,而米尔贝肟/吡喹酮片组的犬在D7和D14时仍有眼线虫检出(即第二次治疗后的一周)。这些数据与之前的研究是一致的,即在使用米尔贝肟/吡喹酮片单次或两次治疗后的效果分别是第7天为72.7%和第14天为90.9%[19]。单次使用10%吡虫啉和2.5%莫昔克丁治疗眼线虫感染的犬,第5天有效率为90.47%,至第9天有效率为95.23%[20]。在本试验中,单次使用10%吡虫啉和2.5%莫昔克丁7天后,除去被感染动物眼睛内眼线虫的有效率为100%,而米尔贝肟/吡喹酮片组需要两次用药后,第21天时才能100%治愈眼线虫感染的犬。莫昔克丁通过皮肤吸收,在犬用药后约4-9天达到最大血药浓度。从皮肤吸收后,莫昔克丁分布于全身,并慢慢从血浆中代谢,表现为在一个月的治疗期间内血浆中仍可检测到莫昔克丁浓度[21]。
每月使用米尔贝肟和10%吡虫啉/2.5%莫昔克丁降低眼线虫感染的有效率分别为90%和100%。所以10%吡虫啉/2.5%莫昔克丁滴剂可以有效治疗和预防犬眼线虫感染。考虑到地区的流行性,例如在意大利南部的一些城市,感染流行率可能高达60%,对动物的持续用药是控制感染的关键,也可以降低影响人类健康的风险。与此同时,对于从非流行地区到流行地区的犬,对眼线虫的感染必须做好预防。反之亦然,变色绕眼果蝇是结膜吸吮眼线虫的传播媒介,在非流行区域必须限制变色绕眼果蝇的引入[22]。与对照组相比,10%吡虫啉和2.5%莫昔克丁滴剂治疗犬结膜吸吮眼线虫的安全性,没有任何不良反应和临床症状。
结论
在欧洲允许广泛使用Advocate®治疗犬寄生虫感染(如猫栉首蚤,犬疥螨,犬蠕形螨,血管圆线虫,犬弓首蛔虫和狭头钩虫),也可以预防犬恶丝虫和匐行恶丝虫的感染,所以可以推荐使用此配方治疗犬结膜吸吮眼线虫感染。最后,由于欧洲报告的动物和人类感染眼线虫的病例越来越多,所以预防和治疗被感染的狗对于控制这种人畜共患病感染至关重要。
文章来源:Domenico Otranto; Vito Colella (2016). Effificacy of moxidectin 2.5% and imidacloprid 10% in the treatment of ocular thelaziosis by Thelazia callipaeda in naturally infected dogs.Veterinary Parasitology 227 (2016) 118–121.
参考文献
[1] Bianciardi, P., Otranto, D., 2005. Treatment of dog thelaziosis caused by Thelazia callipaeda (Spirurida, Thelaziidae) using a topical formulation of imidacloprid 10% and moxidectin 2.5%. Vet. Parasitol. 129, 89–93.
[2] Colella, V., Kirkova, Z., Fok, É., Mihalca, A.D., Tasi´c-Otaˇsevi´c, S., Hodˇzi´c, A.,Dantas-Torres, F., Otranto, D., 2016. Increase in eyeworm infections in Eastern Europe. Emerg. Infect. Dis. 22, 1513–1515.
[3] Diakou, A., Di Cesare, A., Tzimoulia, S., Tzimoulias, I., Traversa, D., 2015. Thelazia callipaeda (Spirurida: Thelaziidae): fifirst report in Greece and a case of canine infection. Parasitol. Res. 114, 2771–2775.
[4] Ferroglio, E., Rossi, L., Tomio, E., Schenker, R., Bianciardi, P., 2008. Therapeutic and prophylactic effificacy of milbemycin oxime (Interceptor) against Thelazia callipaeda in naturally exposed dogs. Vet. Parasitol. 154, 351–353.
[5] Fuentes, I., Montes, I., Saugar, J.M., Latrofa, S., Gárate, T., Otranto, D., 2012. Thelaziosis in humans, a zoonotic infection, Spain, 2011. Emerg. Infect. Dis. 18, 2073–2075.
[6] Hodˇzi´c, A., Latrofa, M.S., Annoscia, G., Ali´c, A., Beck, R., Lia, R.P., Dantas-Torres, F., Otranto, D., 2014. The spread of zoonotic Thelazia callipaeda in the Balkan area. Parasites Vectors 30, 352.
[7] Lechat, C., Siméon, N., Pennant, O., Desquilbet, L., Chahory, S., Le Sueur, C., Guillot, J., 2015. Comparative evaluation of the prophylactic activity of a slow-release insecticide collar and a moxidectin spot-on formulation against infection in naturally exposed dogs in France. Parasites Vectors 8, 93.
[8] Lia, R.P., Traversa, D., Agostini, A., Otranto, D., 2004. Field effificacy of moxidectin 1 per cent against Thelazia callipaeda in naturally infected dogs. Vet. Rec. 154, 143–145.
[9] Máca, J., Otranto, D., 2014. Drosophilidae feeding on animals and the inherent mystery of their parasitism. Parasites Vectors 4, 516.
[10] Motta, B., Schnyder, M., Solari Basano, F., Nägeli, F., Nägeli, C., Schiessl, B., Mallia, E., Lia, R.P., Dantas-Torres, F., Otranto, D., 2012. Therapeutic effificacy of milbemycin oxime/praziquantel oral formulation (Milbemax®) against Thelazia callipaedain naturally infested dogs and cats. Parasites Vectors 19, 85.
[11] Otranto, D., Dutto, M., 2008. Human Thelaziasis, Europe. Emerg. Infect. Dis. 14, 647–649
[12] Otranto, D., Ferroglio, E., Lia, R., Traversa, D., Rossi, L., 2003a. Current status and epidemiological observations of Thelazia callipaeda (Spirurida, Thelaziidae) in dogs, cats and foxes in Italy: a coincidence or a parasitic disease of the old continent? Vet. Parasitol. 116, 315–325
[13] Otranto, D., Lia, R.P., Traversa, D., Giannetto, S., 2003b. Thelazia callipaeda (Spirurida, Thelaziidae) of carnivores and humans: morphological study by light and scanning electron microscopy. Parassitologia 45, 125–133.
[14] Otranto, D., Cantacessi, C., Testini, G., Lia, R.P., 2006. Phortica variegata as an intermediate host of Thelazia callipaeda under natural conditions: evidence for pathogen transmission by a male arthropod vector. Int. J. Parasitol. 36, 1167–1173.
[15] Otranto, D., Dantas-Torres, F., Mallia, E., DiGeronimo, P.M., Brianti, E., Testini, G., Traversa, D., Lia, R.P., 2009. Thelazia callipaeda (Spirurida, Thelaziidae) in wild animals: report of new host species and ecological implications. Vet. Parasitol. 166, 262–267.
[16] Otranto, D., Cantacessi, C., Dantas-Torres, F., Brianti, E., Pfeffer, M., Genchi, C., Guberti, V., Capelli, G., Deplazes, P., 2015. The role of wild canids and felids in spreading parasites to dogs and cats in Europe. Part II: Helminths and arthropods. Vet. Parasitol. 213, 24–37.
[17] Paradˇzik, M., Samardˇzi´c, K., ˇ Ziviˇcnjak, T., Martinkovi´c, F.,ˇZ. Janjetovi´c, Mileti´c-Medved, M., 2016. Thelazia callipaeda-fifirst human case of thelaziosis in Croatia. Wien. Klin. Wochenschr. 128, 221–223.
[18] Rossi, L., Bertaglia, P., 1989. Presence of Thelazia callipaeda Railliet and Henry 1910, in Piedmont, Italy. Parassitologia 31, 167–172.
[19] Rossi, L., Peruccio, C., 1989. Thelaziosi oculare nel Cane: aspetti clinici e terapeutici. Veterinaria 2, 47–50.
[20] Shen, J., Gasser, R.B., Chu, D., Wang, Z.X., Yuan, X., Cantacessi, C., Otranto, D., 2006. Human thelaziosis—a neglected parasitic disease of the eye. J. Parasitol. 92, 872–875
[21] Skrjabin, K.I., Sobolov, A.A., Ivashkin, V.M., 1971. Essentials of nematodology. Spirurata of Animals and Man and the Diseases Caused by Them, Part 4 Thelazioidea, Vol. 16. Israel Program for Translations, Jerusalem, Israel (ISBN 978-0706511796).
[22] Tasi´c-Otaˇsevi´c, S., Gabrielli, S., Trenki´c-Boˇzinovi´c, M., Petrovi´c, A., Gaji´c, B., Colella, V., Momˇcilovi´c, S., Cancrini, G., Otranto, D., 2016. Eyeworm infections in dogs and in a human patient in Serbia: a one health approach is needed. Comp. Immunol. Microbiol. Infect. Dis. 45, 20–22.