农业农村部公告 第690号 | 批准9家单位申报的2种兽药产品注册
农业农村部公告 第690号
根据《兽药管理条例》和《兽药注册办法》规定,经审查,批准中国动物卫生与流行病学中心等9家单位申报的非洲猪瘟病毒(P72/CD2v/MGF)三重荧光PCR检测试剂盒等2种兽药产品注册,并发布产品工艺规程、质量标准、说明书和标签。自发布之日起执行。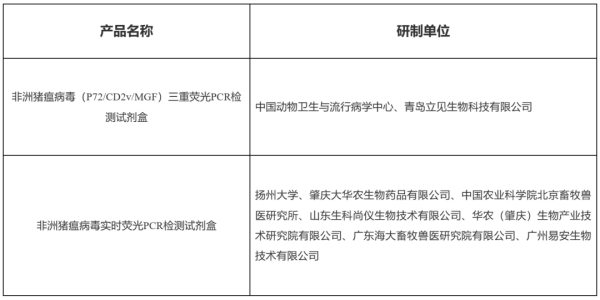
附件2(略)
附件3(略)
附件4
说明书和标签
一、非洲猪瘟病毒(P72/CD2v/MGF)三重荧光PCR检测试剂盒说明书和内包装标签(一)非洲猪瘟病毒(P72/CD2v/MGF)三重荧光PCR检测试剂盒说明书 通用名 非洲猪瘟病毒(P72/CD2v/MGF)三重荧光PCR检测试剂盒 英文名 African swine fever virus(P72/CD2v/MGF)Triple Real–Time PCR Test Kit 汉语拼音 Feizhouzhuwenbingdu(P72/CD2v/MGF)Sanchong Yingguang PCR Jianceshijihe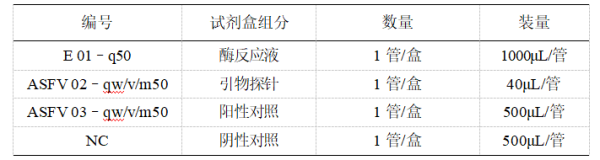
【作用与用途】 用于全血、血清、淋巴结、脾脏、肾脏、扁桃体、肌肉、唾液、精液、口鼻拭子、肛拭子和环境拭子等样品中的非洲猪瘟病毒P72基因、CD2v基因和MGF 505–1R基因的检测。1.1.1 活猪样品 全血、血清、唾液、精液各5 ml。1.1.2 拭子样品 口鼻拭子、肛拭子和环境拭子浸入5ml PBS缓冲液中。1.1.3 病死猪剖检样品或屠宰场剖检样品 采集死猪的淋巴结、脾脏、肾脏、扁桃体、肌肉等组织样品。2~8℃低温运至实验室用于检测。1.2.1 活猪样品处理方法 直接取200μL全血、血清、唾液、精液进行核酸提取。1.2.2 淋巴结、脾脏、肾脏、扁桃体、肌肉等组织样品处理方法 取50mg的组织块放入盛有0.5ml PBS缓冲液的研磨管中,6000r/min振荡研磨45s,制成约10%的组织匀浆液,5000r/min离心5分钟,取200μL上清液进行核酸提取。1.2.3 拭子样品处理方法 振荡数次,取200μL上清液进行核酸提取。1.2.4 样品核酸提取 采用DNA纯化试剂盒或自动核酸提取仪提取各类样品中的核酸。1.3.1 将引物探针(棕色管)和酶反应液瞬时离心后,将酶反应液全部移至引物探针(棕色管)中,颠倒混匀6次,充分混匀,配制成PCR反应液。1.3.2 根据检测样品数量每个PCR反应管加入20μL PCR反应液;先取5μL阴性对照、再取5μL待检 DNA、最后取5μL阳性对照(充分混匀)分别加到不同的PCR反应管中,加样结束后应盖紧PCR反应管,每个PCR反应管内液体的体积为25μL。1.4 PCR反应 加样后将PCR反应管瞬时离心,然后置于荧光PCR仪内,进行如下反应:37℃孵育2分钟;95℃预变性20秒;95℃变性10秒,60℃延伸30秒,共40个循环;设置60℃收集FAM、VIC与Cy5荧光信号。1.5 结果分析 采用仪器设备默认的自动分析方法,计算P72基因、CD2v基因和MGF基因荧光PCR反应Ct值。2.1 结果的有效性 FAM信号、VIC信号和Cy5信号通道下,阳性对照同时应出现典型扩增曲线且Ct 值<35,且阴性对照无典型扩增曲线或无Ct值,则试验成立;否则试验不成立。2.2.1 非洲猪瘟病毒P72基因 FAM信号通道下,当样品的扩增结果有典型的扩增曲线且Ct值<37时,判定为非洲猪瘟病毒P72基因阳性。当样品的扩增结果无Ct值或无典型的扩增曲线时,可初步判定为非洲猪瘟病毒P72基因阴性;当样品的扩增结果有典型的扩增曲线且37≤Ct值<40时,可初步判定为非洲猪瘟病毒P72基因可疑;对初步判定阴性样品或可疑样品应再进行1次复检,做3个重复反应,若1、2或3个重复反应的Ct值<40,且出现典型的扩增曲线,最终判定为非洲猪瘟病毒P72基因阳性,扩增结果无Ct值或无典型的扩增曲线时,最终判定为非洲猪瘟病毒P72基因阴性。2.2.2 非洲猪瘟病毒CD2v基因 VIC信号通道下样品的扩增结果有典型的扩增曲线且Ct值<37时,判定为非洲猪瘟病毒CD2v基因阳性。当样品的扩增结果无Ct值或无典型的扩增曲线时,可初步判定为非洲猪瘟病毒CD2v基因阴性;当样品的扩增结果有典型的扩增曲线且37≤Ct值<40时,可初步判定为非洲猪瘟病毒CD2v基因可疑;对初步判定阴性样品或可疑样品应再进行1次复检,做3个重复反应,若1、2或3个重复反应的Ct值<40,且出现典型的扩增曲线,最终判定为非洲猪瘟病毒CD2v基因阳性,扩增结果无Ct值或无典型的扩增曲线时,最终判定为非洲猪瘟病毒CD2v基因阴性。2.2.3 非洲猪瘟病毒MGF基因 Cy5信号通道下样品的扩增结果有典型的扩增曲线且Ct值<37时,判定为非洲猪瘟病毒MGF基因阳性。当样品的扩增结果无Ct值或无典型的扩增曲线时,可初步判定为非洲猪瘟病毒MGF基因阴性;当样品的扩增结果有典型的扩增曲线且37≤Ct值<40时,可初步判定为非洲猪瘟病毒MGF基因可疑;对初步判定阴性样品或可疑样品应再进行1次复检,做3个重复反应,若1、2或3个重复反应的Ct值<40,且出现典型的扩增曲线,最终判定为非洲猪瘟病毒MGF基因阳性,扩增结果无Ct值或无典型的扩增曲线时,最终判定为非洲猪瘟病毒MGF基因阴性。(1)ABI荧光定量PCR仪(ABI QuantStudio5)的FAM、VIC和Cy5三通道互不影响,在程序设置时,请将仪器参数“Passive Reference”设置为“None”。(2)伯乐荧光定量PCR仪(CFX–96)需与阳性对照检测的荧光信号和Ct值同步进行分析。(3)罗氏480荧光定量PCR仪(LightCycler480 II)进行结果分析时需选择“Abs Quant/Fit Points”分析方法,并将“Background”设置为“3–15”或通过建立颜色补偿文件再对荧光PCR扩增结果进行分析。(4)其它仪器设备需根据仪器的效能可进行适当的颜色补偿。(5)使用本试剂盒的试验室应严格按照国家有关规定进行管理。(6)酶反应液、引物探针配置成的PCR反应液对温度敏感容易失活,使用时应置于冰上,使用后应立即冻存,每盒反应液冻融次数不宜超过3次。(7)扩增试剂准备时应按阴性对照、待检核酸、阳性对照的顺序加入PCR反应管中。(8)吸取反应液时,应尽量避免产生气泡;加样结束后应盖紧反应管,以免液体蒸发造成结果不准确。(9)处理样品用器械及废弃物品应高压灭菌。检测过程中使用过的吸头,应直接打到盛有10%84消毒液的带盖废物缸内。检测结束的PCR反应管,严禁开盖不得高压处理。(10)工作台及各种试验用品应定期清洁并用10%84消毒液或紫外灯进行防污染处理。(11)各区域物品均为专用,不得交叉使用,以免污染。检测结束后,应立即对工作台进行清洁。(12)严禁使用超过有效期限的试剂;不同批号的试剂请勿混用。【贮藏与有效期】 –20℃以下保存,有效期为15个月。(二)非洲猪瘟病毒(P72/CD2v/MGF)三重荧光PCR检测试剂盒内包装标签非洲猪瘟病毒(P72/CD2v/MGF)三重荧光PCR检测试剂盒【作用与用途】 详见说明书。用于全血、血清、淋巴结、脾脏、肾脏、扁桃体、肌肉、唾液、精液、口鼻拭子、肛拭子和环境拭子等样品中的非洲猪瘟病毒P72基因、CD2v基因和MGF 505–1R基因的检测。【贮藏与有效期】 –20℃以下保存,有效期为15个月。【贮藏与有效期】 –20℃以下保存,有效期为15个月。【贮藏与有效期】 –20℃以下保存,有效期为15个月。【贮藏与有效期】 –20℃以下保存,有效期为15个月。【贮藏与有效期】 –20℃以下保存,有效期为15个月。二、非洲猪瘟病毒实时荧光PCR检测试剂盒说明书和内包装标签 汉语拼音 Feizhouzhuwenbingdu Shishi Yingguang PCR Jiance Shijihe 英文名称 Real–Time Fluorescence PCR Detection Kit for African Swine Fever Virus 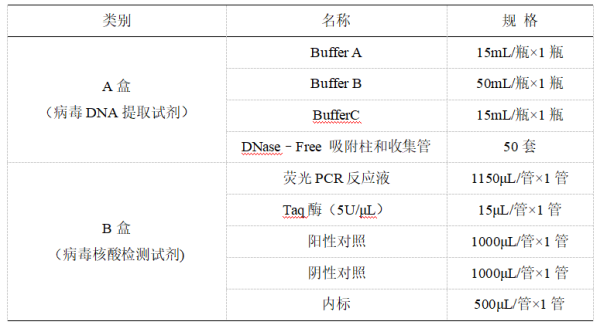
【作用与用途】 用于检测血液、血球粉、淋巴结、脾脏、扁桃体中非洲猪瘟病毒核酸。1.1.1 淋巴结、脾脏、扁桃体样品 用无菌剪刀和镊子剪取待检样品2g于研钵中充分研磨,再加10mL PBS(pH 7.2)混匀(样品不足2g按1∶5比例加PBS),3,000 r/min,4℃离心5分钟,取上清液,编号备用。1.1.2血球粉样品 取100mg样品直接加1mL PBS(pH 7.2)混匀(样品不足2g按1∶5比例加PBS),3,000 r/min,4℃离心5分钟,取上清液,编号备用。1.1.4 样品保存 采集或处理好的样品在2℃~8℃条件下保存不超过72h;若需长期保存,须放置–80℃保存,避免反复冻融。使用前请先在Buffer A中加入异丙醇15mL、Buffer B中加入无水乙醇50mL。(1)待检样品、阳性对照和阴性对照的份数总和为n,取n个灭菌的1.5mL离心管,一一编号。(3)每管分别加入已处理的待检样品、阳性对照、阴性对照各200μL。(4)每管加入内标10μL,充分混匀,室温放置10min。(5)取与上述离心管等数量的DNase–Free吸附柱和收集管,编号后将离心管中的溶液转移至DNase–Free吸附柱,为避免堵塞吸附柱,尽量不要吸悬浮杂质。(8)吸附柱内加入600μL Buffer B,12,000 r/min离心1分钟。(11)12,000 r/min空柱离心2分钟,去除残留液。(12)将每个吸附柱分别移入新的1.5mL离心管中,向柱中央加入100μL Buffer C,室温静置2分钟,12,000 r/min离心1分钟,离心管中液体即为模板DNA溶液。提取的DNA溶液冰上保存备用(注意:提取的DNA溶液须在2小时内进行PCR 扩增,若需长期保存须放置–80℃保存,避免反复冻融)。从试剂盒中取出PCR反应液和Taq酶,在室温下融化,振荡均匀后,2,000rpm离心5秒。设所需PCR反应管数为n(n =样品数+ 1管阴性对照+ 1管阳性对照),每个测试反应体系配制如表2。 计算好各试剂的使用量,加入一适当体积离心管中,充分混合均匀,2,000 rpm离心10秒,向设定的n个反应管中分装23μL,转移至样品处理区。n个PCR反应管中分别加入上述1.2.1中提取的DNA溶液2μL,反应体系为25μL,盖紧管盖,混匀,离心机瞬时离心后,将PCR 反应管转移至检测区,置于实时荧光PCR仪上,记录样品摆放顺序。扩增条件:94℃ 3min;94℃ 5sec,60℃ 30sec(收集荧光),45个循环。ASFV荧光信号收集时设定为FAM荧光素,内标荧光信号收集时设定为VIC荧光素(如机器没有VIC荧光素,则选择HEX荧光素),参比荧光选为none。(4)核酸扩增适用下列仪器类型:ABI 7500/7300、Roche LightCycler 480、Rotor–Gene Q、SLAN等实时荧光PCR仪。阈值设定 根据仪器噪声情况进行调整,以阈值线刚好超过阴性对照品扩增曲线的最高点为准。呈现S型曲线,内标基因的CT值(VIC/HEX通道)应≤32.0;呈现S型曲线,阳性对照的CT值(FAM通道)应≤28.0。呈现S型曲线,CT值(FAM通道)≤38.0的样品判为阳性。呈现S型曲线,CT值(FAM通道)>38.0的样品建议重做;如重做结果CT值(FAM通道)为none的判为阴性,有数值则判为阳性。(1)本试剂盒仅供兽医及相关专业人士使用,试剂盒中各组分应避免反复冻融。(2)实验室应至少分三个区:样品处理区、PCR前准备区和检测区。(3)各区物品均为专用,不得交叉使用,避免污染;检测结束后,应立即对工作台进行清洁;工作台及各种实验用品应定期用1%次氯酸钠、75%酒精或紫外灯进行消毒。(4)在整个检测过程中应注意避免交叉污染,提取核酸时应用灭菌的镊子夹取离心管;离心管开盖时应避免粘在手上或溅出,否则要立即更换手套。(5)Buffer A有腐蚀性,切勿沾到皮肤或衣服上,一旦沾上应立即用大量清水冲洗并擦干。(6)反应液在使用前要彻底融化,反应液与Taq酶混合后需瞬时离心将液体甩至管底;分装反应液时,应尽量避免产生气泡;上机前注意检查各反应管是否盖紧,以免荧光物质泄露污染仪器。(7)阳性对照在吸取前应在微量漩涡振荡器上振荡1–2sec。(8)对样品及其废弃物的操作应严格遵守生物安全规定。【贮藏与有效期】 A盒(病毒DNA提取试剂)室温保存,B盒(病毒核酸检测试剂)–20℃保存,有效期均为12个月。(二)非洲猪瘟病毒实时荧光PCR检测试剂盒内包装标签【贮藏与有效期】 –20℃保存,有效期为12个月。【贮藏与有效期】 –20℃保存,有效期为12个月。【贮藏与有效期】 –20℃保存,有效期为12个月。【贮藏与有效期】 –20℃保存,有效期为12个月。【贮藏与有效期】 –20℃保存,有效期为12个月。【贮藏与有效期】 –20℃保存,有效期为12个月。