来源:兽药产业技术创新联盟
近日,中国农业科学院哈尔滨兽医研究所研究发现,核苷酸糖转运蛋白SLC35B4介导的硫酸乙酰肝素修饰信号通路在流感病毒高效内化进入宿主细胞的过程中发挥重要作用,相关研究成果于近日发表在《mBio》上。
蛋白糖基化修饰主要分为N-糖基化和O-糖基化修饰,在病毒入侵过程中发挥至关重要的作用。其中,N-糖基化修饰的唾液酸已被证实是流感病毒的吸附受体;O-糖基化修饰在病毒学研究中最为广泛的是硫酸乙酰肝素修饰,其参与新冠病毒、登革热病毒、丙肝病毒等多种病毒的入侵细胞过程。但是,硫酸乙酰肝素修饰信号通路是否参与介导流感病毒的入侵过程仍未可知。
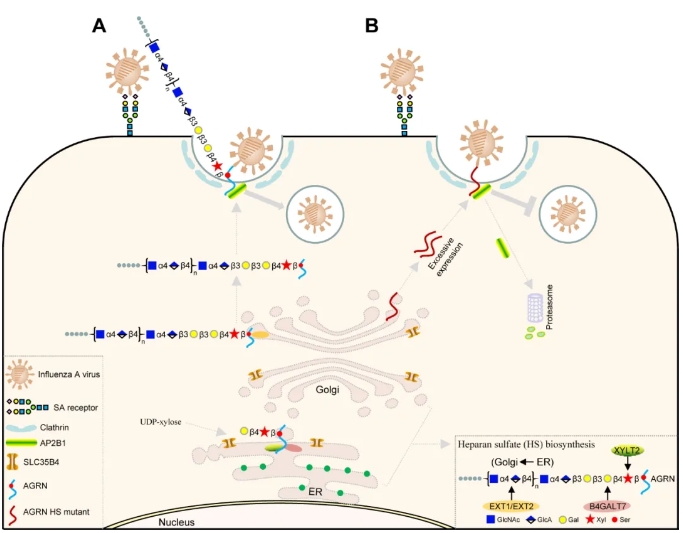
该研究发现,体外下调或缺失SLC35B4表达后能够抑制不同亚型流感病毒复制;同时,在小鼠体内干扰下调SLC35B4表达后能够使60%的小鼠抵御WSN(H1N1)病毒的致死性攻击。机制解析时发现,核苷酸糖转运蛋白SLC35B4将UDP-Xylose由细胞质转运至内质网中,XYLT2催化UDP-Xylose偶联到硫酸乙酰肝素修饰蛋白AGRN的丝氨酸残基上,随后B4GALT7-EXT1/EXT2等催化硫酸乙酰肝素链延长,最终硫酸乙酰肝素修饰蛋白AGRN被转运至细胞膜,辅助流感病毒招募下游分子入侵宿主细胞。硫酸乙酰肝素修饰蛋白AGRN与流感病毒囊膜蛋白血凝素(HA)的HA1亚基互作,进而招募AP2B1启动内化过程;当SLC35B4蛋白缺失后使得未被硫酸乙酰肝素修饰的AGRN过量累积,导致AP2B1经泛素蛋白酶体途径降解,从而抑制流感病毒的内化过程。该研究最终阐明SLC35B4-XYLT2-B4GALT7-EXT1-EXT2-AGRN-AP2B1信号轴介导流感病毒内化过程的分子机制。
动物流感基础与防控研究创新团队王广文副研究员为论文的第一作者,陈化兰院士和李呈军研究员为论文的共同通讯作者。该研究得到国家重点研发计划项目(2021YFD1800203、2021YFD1800204)、国家自然科学基金项目(32272979、32192453、32172847)、黑龙江省杰青项目(JQ2023C006)及中国农业科学院基础研究科学中心项目(CAAS-CSLPDCP-202401)等资助。
原文链接:https://journals.asm.org/doi/10.1128/mbio.00194-25